Verordening (EU) 2017/542 (CLP bijlage VIII) is nieuw en roept veel vragen op. Getracht wordt een verduidelijking te geven – update december 2020.
Voor welke mengsels is de productnotificatie verplicht?
Mengsels welke een classificatie met gezondheid- en fysische gevaren hebben dienen te worden genotificeerd conform verordening (EU) 2017/542.
Welke mengsels zijn vrijgesteld van productnotificatie?
Vrijgesteld zijn stoffen en de volgende mengsels:
- Niet geclassificeerde mengsels;
- Gassen onder druk;
- Ontplofbare stoffen (klasse 1.1 – 1.6);
- Radioactieve stoffen;
- Cosmetica;
- Mengsel voor onderzoek (PPORDs);
- Mengsels met enkel een milieuclassificatie.
Zijn artikelen vrijgesteld van productnotificatie?
Artikelen zijn vrijgesteld van de notificatieplicht behalve als een artikel wordt gecombineerd met een mengsel zoals auto accu’s, kaarsen, schoonmaakdoekjes.
Zijn oplossingen vrijgesteld van productnotificatie?
Een (geclassificeerde) oplossing bijvoorbeeld van een stof in water, wordt gezien als een mengsel en is niet vrijgesteld.
Welke vrijstelling krijgen mengsels welke < 2021 al zijn genotificeerd in betreffend land?
Deze mengsels mogen/moeten worden voorzien van een UFI echter de gegevens volgens de bijlage van verordening (EU) 2017/542 zijn vrijgesteld tot 1 januari 2025 (mits geen product of classificatie wijzigingen).
Wanneer moet de productnotificatie voor een mengsel worden gedaan?
Dat is afhankelijk voor wie het mengsel bedoeld is:
- ≤ 1 januari 2021 voor mengsels voor gebruik door consumenten (eerder was dit 2020);
- ≤ 1 januari 2021 voor mengsels voor beroepsmatig gebruik;
- ≤ 1 januari 2024 voor mengsels voor industrieel gebruik.
Wordt het mengsel gebruik voor verschillende doelgroepen dan is de vroegste datum van toepassing.
De ECHA database is vanaf 24 april 2019 opengesteld voor notificatie (notificatie per land is in opbouw). Verder is er een validatie assistent beschikbaar voor het controleren van de geldigheid van informatie.
Wanneer moet het geregeld zijn?
Als bedrijf mag u enkel nieuwe/gewijzigde producten met een UFI op de markt brengen, afhankelijk van de doelgroep is het advies om ruim van te voren te starten om etiketaanpassingen van voorraden te voorkomen.
Wat is het proces van productnotificatie?
Eerst een UFI verkrijgen op de website van ECHA (https://ufi.echa.europa.eu/#/create) en vervolgens een notificatie op de ECHA website of indien het land dit vereist op een nationale website.
Welke gegevens worden gevraagd?
Voor productnotificatie de volgende gegevens:
- volledige chemische samenstelling;
- toxicologische informatie;
- etiket gegevens;
- product categorie indeling (EuPCS);
- Detail gegevens van het product (o.a. handelsnaam);
- Aanvullende gegevens (verpakking, kleur,…);
- UFI.
Voor welke landen gebruik kan worden gemaakt van de centrale ECHA registratie?
Dit is nog in ontwikkeling en aan het land zelf om te beslissen of registratie mogelijk is via de ECHA website en/of via een nationale toegang. Vooralsnog hebben alle landen aangegeven positief te staan tegenover de centrale ECHA oplossing waarbij enkele landen hebben aangegeven dat een alternatieve nationale oplossing mogelijk blijft.
Tot welk percentage mag gebruik worden gemaakt van mixture in mixture?
Tot 100 %.
Wat als de mixture in mixture (MIM) grondstofmengsel is genotificeerd in een ander land dan waarop het mengsel op de markt wordt gebracht?
De gifcentra hebben (vooralsnog) geen inzage in gegevens welke in een ander land zijn genotificeerd vandaar dat naast UFI gegevens ook grondstofinformatie vereist is van mixture in mixture.
Wat als de volledige mengsel gegevens van de MIM ontbreken?
Indien de MIM inhoudsgegevens niet volledig zijn moet informatie over de bekende mengselbestanddelen overeenkomstig rubriek 3 van het veiligheidsinformatieblad worden verstrekt aangevuld met de concentratie en de UFI, indien beschikbaar. Bij gebrek aan een UFI wordt het veiligheidsinformatieblad van de MIM verstrekt, alsmede de naam, het e-mailadres en het telefoonnummer van de leverancier. Tenslotte de classificatie en etiket gegevens.
Volstaan de gegevens vanuit het veiligheidsinformatieblad?
Naast de gegevens vanuit het veiligheidsinformatieblad worden receptuur gegevens gevraagd van geclassificeerde en niet geclassificeerde inhoudsstoffen. Eveneens moeten gegeven van de verpakking worden verstrekt (als niet industrieel gebruik).
Is er een ondergrens voor de opgave van gegevens van niet geclassificeerde inhoudsstoffen?
De gegevens van niet geclassificeerde inhoudsstoffen moeten worden vermeld vanaf een percentage van 1 %.
Mag het veiligheidsinformatieblad als bijlage worden ge-upload in de notificatie database en naar worden verwezen in de notificatie?
Het doel van de database is dat deze doorzoekbaar is, voor consumenten en beroepsmatig gebruik is deze werkwijze niet gewenst.
Moeten alle receptuurgegevens worden gegeven of zijn er uitzonderingen?
Er is een uitzondering voor bestanddelen voor geur, reuk of kleur op voorwaarde dat:
- de mengselbestanddelen niet voor enig gezondheidsgevaar zijn ingedeeld (voor geur- of reukbestanddelen die niet zijn ingedeeld of alleen voor sensibilisatie van de huid categorie 1, 1A of 1B of aspiratietoxiciteit zijn ingedeeld);
- geur- of reukstoffen op voorwaarde dat de totale concentratie van geur- en reukstoffen in het mengsel niet meer dan 5 % bedraagt en;
- 25 % voor de som van de kleurstoffen.
Moeten voor alle componenten exacte percentages van de receptuur worden opgegeven?
Exacte percentages in afnemende volgorde per massa of volume zijn verplicht voor componenten met de volgende classificatie:
- acute toxiciteit, categorie 1, 2 of 3;
- specifieke doelorgaantoxiciteit bij eenmalige blootstelling, categorie 1 of 2;
- specifieke doelorgaantoxiciteit bij herhaalde blootstelling, categorie 1 of 2;
- huidcorrosie, categorie 1, 1A, 1B of 1C;
- ernstig oogletsel, categorie.
Als alternatief voor de indiening van concentraties in exacte percentages mag een percentagebereik:
Concentratiebereik van het gevaarlijke bestanddeel in het mengsel (%) – Maximale reikwijdte van het concentratiebereik voor de indiening:
- ≥ 25 – < 100 – 5 procentpunten;
- ≥ 10 – < 25 – 3 procentpunten;
- ≥ 1 – < 10 – 1 procentpunt;
- ≥ 0,1 – < 1 – 0,3 procentpunten;
- > 0 – < 0,1 – 0,1 procentpunt.
De percentage gegevens voor andere gevaarlijke bestanddelen en niet als gevaarlijk ingedeelde bestanddelen (m.u.v. kleur, geur en reukstoffen):
Concentratiebereik van het bestanddeel in het mengsel (%) – Maximale reikwijdte van het concentratiebereik voor de indiening:
- ≥ 25 – < 100 – 20 procentpunten;
- ≥ 10 – < 25 – 10 procentpunten;
- ≥ 1 – < 10 – 3 procentpunten;
- > 0 – < 1 – 1 procentpunt.
Concentraties lager dan 0,1 % zijn verplicht, tenzij de indiener aantoont dat deze bestanddelen irrelevant zijn in verband met de respons in noodgevallen met betrekking tot de gezondheid en preventieve maatregelen.
Mengselbestanddelen in concentraties gelijk aan of hoger dan 1 % welke op basis van hun gevolgen voor de gezondheid of hun fysische effecten niet als gevaarlijk zijn ingedeeld moeten worden inbegrepen.
In het geval van een beperkte indiening kan de te verstrekken informatie over de samenstelling van een mengsel voor industrieel gebruik worden beperkt tot de informatie op het veiligheidsinformatieblad, op voorwaarde dat aanvullende informatie over de samenstelling overeenkomstig op verzoek snel beschikbaar is.
Hoe moet de concentratiebereik in procenten worden gelezen voor de opgave van productgegevens?
Stel een 6 % component is aanwezig in een mengsel dan is de maximale concentratie variatie volgens tabel 2 van verordening (EU) 2017/542 3 % b.v. 6 – 9 %, 5 – 8 %, 5,5 – 8,5 %.
Hoe moet de concentratiebereik in procenten worden gelezen voor actualisatie van notificatie bij de opgave van productgegevens?
Stel een 5 % component is aanwezig in een mengsel dan is de maximale concentratie variatie volgens tabel 3 van verordening (EU) 2017/542 20 %. Bij een variatie van de concentratie van bestanddelen van ≤ 4 % of ≥ 6 % is in dit geval een actualisering van de indiening vereist.
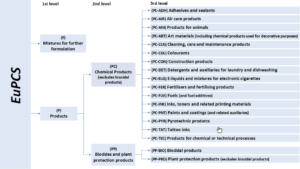
Hoe is het EuPCS systeem opgebouwd?
EuPCS categorie systeem codes zijn alfanumeriek, de categorieën zijn gestructureerd voor de identificatie van het type product of productgroep. Het omvat vier niveau’s.
Een UFI is deze geldig voor de gehele EU?
Gekozen kan worden door de leverancier voor een UFI per land of een groep van landen (ook de gehele EU).
Hoe ziet een UFI er uit?
Een UFI bevat in hoofdletters de naam UFI aangevuld met een 16 karakters unieke alfanumerieke code in 4 blokken b.v. UFI: A300-N06Y-N00U-G73S. Er zit een controle in het nummer. De afkorting “UFI” in hoofdletters, gevolgd door een dubbelepunt (“UFI:”) zijn onderdeel van de aanduiding.
Mogen mengsels welke zijn vrijgesteld (b.v. niet geclassificeerd of enkel een milieuclassificatie) toch een UFI code krijgen?
Deze mengsels mogen worden voorzien van een UFI op vrijwillige basis. Het kan een keuze zijn om uw klant te ondersteunen en vanwege uniformiteit. In dat geval is het verzoek om ook de notificatie gegevens te melden.
Moet de UFI code terugkomen op het veiligheidsinformatieblad?
De UFI code is een etiketelement en mag vermeld te worden in rubriek 1.1. (productidentificatie) van het veiligheidsinformatieblad. In het geval van niet-verpakte gevaarlijke mengsels moet de UFI op het veiligheidsinformatieblad worden vermeld.
Is een UFI code uniek?
Het principe is bij elk uniek mengsel (met enige flexibiliteit) behoort bij één unieke UFI.
Moet de UFI altijd op het etiket?
Voor gevaarlijke mengsels voor industrieel gebruik en mengsels die niet zijn verpakt, mag de UFI op het veiligheidsinformatieblad worden vermeld. De UFI moet op het etiket of mag “bevestigd” worden aan/op het etiket (b.v. stikker).
Wanneer moet de UFI worden gewijzigd?
De UFI moet worden gewijzigd als:
- Een component wordt toegevoegd, vervangen of weggelaten;
- De concentratie van een ingrediënt varieert buiten de gegeven concentratie bereiken;
- De toeleverancier verandert de UFI met gevolg voor de MIM.
Is de productnotificatie een marktbelemmering?
De productnotificatie is vereist om het product (in betreffend EU land) op de markt te brengen. Onduidelijk is nog of het land een goedkeuring van de notificatie moet geven welke mogelijk een vertraging kan geven.
Is er een kwaliteitscheck op de gegevens?
Een kwaliteitscheck bij invoer van de notificatie gegevens per product wordt (automatisch) gedaan door het ECHA portaal middels de validatie assistent en vervolgens door het gifcentrum van het betreffende land van indiening.
Indieningsgegevens bij het ECHA portaal controleert een aantal gegevens automatisch (Validation rules for poison centres notifications b.v. versie 4.1) met als resultaat “succesvol”, “succesvol met waarschuwingen” of “mislukt”.
Wie moet de indiening doen voor de productnotificatie van een product?
Productnotificatie moet gedaan worden door de downstreamgebruik (mengsel producent, her-verpakker, her-vuller, toll-blender) of de importeur. Deze taak ligt niet bij de producent van stoffen of de distributeur (her-labelen, private label, handelaar). Wel moet gegarandeerd zijn dat in de notificatiedatabase de private label is opgenomen.
Voor mengsels voor industrieel gebruik bestaat onder voorwaarden de mogelijkheid voor een beperkte indiening. Staan alle voorwaarden in Verordening (EU) 2017/542?
Indien het mengsel voor industrieel gebruik wordt verwerkt in een product b.v. voor consumenten gebruik vervalt deze beperkte indiening.
Wie is juridisch verantwoordelijk voor de notificatie?
Een distributeur (ondanks dat men b.v. een private label gebruikt) is juridisch niet aansprakelijk, deze verantwoording blijft bij de producent of importeur van het mengsel.
Hoe staat import in deze?
Import staat gelijk met op de markt plaatsen.
Waar moet de notificerende organisatie zijn gevestigd?
In de Europese Unie.
Wat als de juridische entiteit van het bedrijf verandert?
De notificatie moet bij verandering van de juridische entiteit opnieuw worden ingediend. Een kopieerfunctie is beschikbaar.
Wat zijn de kosten voor notificatie?
De kosten voor notificatie overeenkomstig artikel 45, lid 1, van Verordening (EG) nr. 1272/2008 variëren nu al per land van nihil tot een bijdrage. Verordening (EU) 2017/542 doet hier geen uitspraak over.
Zijn er taal specifieke eisen bij de invoer van de gegevens voor productnotificatie?
De gegevens van rubriek 11 van het veiligheidsinformatieblad zijn taal specifiek, voor het land waar het product op de markt wordt gebracht dient deze in de officiële taal (talen) te worden ingevuld. De discussie is nog open of (een tiental) landen Engels accepteren.
Moet het veiligheidsinformatieblad worden bijgevoegd?
Dit is optioneel mogelijk voor het mengsel product en verplicht voor een MIM indien de UFI hiervoor ontbreekt.
Waarvoor mogen de lidstaten de informatie van de productnotificatie gebruiken?
Enkel voor preventieve en curatieve maatregelen (noodgevallen) en statistische analyse (risicobeheersmaatregelen) – referentie EG Verordening 1272/2008 artikel 45.
De informatie mag niet voor andere doeleinden worden gebruikt (dus niet voor b.v. marktinformatie, toezicht, politiek).
In de aanvraag van een UFI wordt gevraagd om een BTW nummer, welke eis is hieraan gesteld?
Het BTW nummer (in Nederland BTW-id) in de aanvraag van een UFI mag afwijken van het BTW nummer van het bedrijf welke het product op de markt brengt.
Waar staan de in productnotificatie gebruikte afkortingen voor?
EuPCS – European Product Categorisation System.
PCN – Poison Centres Notification.
MIM – Mixture in mixture (mengsel in mengsel).

UFI – Unieke formule-identificatie(s).
Vervalt het i-teken?
Het i-teken volgens EN 15178:2007 is vanaf 2021 niet langer geldig en vervangen door een UFI (b.v. UFI: JY11-Y0MJ-W060-8759).
Waar kan de productnotificatie worden gedaan?
In april 2019 is het centrale portaal geopend door ECHA voor kennisgevingen aan gifcentra.
Is er een handleiding vanuit ECHA?
Zie hiervoor “Richtsnoer over geharmoniseerde informatie in verband met de gezondheid met het oog op respons in noodgevallen – Bijlage VIII bij de CLP-verordening” (NL versie 3.0).
Zijn er uitzonderingen voor specifieke producten?
Er zijn specifieke regels voor op wens bereide verf, gipsbindmiddel, cement en brandstoffen.
Liggen de invoeringsdata van deze wetgeving vast?
Middels een publieke consultatie heeft in de EU een discussie gelopen voor uitstel van de startdatum van 1 januari 2020 naar 1 januari 2021. In vervolg hierop heeft de Caracal CLP expert groep in september 2019 voorgesteld om de datum voor informatieverstrekking voor consumenten producten te verzetten naar 2021. De Europese Commissie heeft dit in november 2019 aangenomen. Andere implementatiedatums zijn niet gewijzigd.
Disclaimer:
Gebruik van enige informatie verkregen middels deze website gebeurt voor risico van de gebruiker. SafetyDocs spant er zich voor in de inhoud van de webpagina regelmatig te actualiseren en/of aan te vullen. Ondanks deze zorg en aandacht is het mogelijk dat de inhoud die middels deze website gevonden wordt, onvolledig en/of onjuist is. SafetyDocs aanvaardt geen enkele aansprakelijkheid voor schade ontstaan uit het bezoeken van deze site of voor enige schade ontstaan vanuit de aangeboden of verwezen content.
SafetyDocs is niet aansprakelijk voor (de gevolgen van) eventuele onvolledigheid of onjuistheid van de informatie. Een bedrijf zelf blijft altijd verantwoordelijk voor het voldoen aan de REACH-/CLP-wetgeving. Het enige wettelijk geldende document is de officiële tekst van de betreffende verordening.